Да ли су и нове вакцине, до скоро непознате широј стручној јавности, део ремећења природне хомеостазе људског организма, питају примаријус др Милан Рогановић и др Марта Ковачевић
Девојка добровољац прима вакцину против ковида-19 у институту у Москви (Фото: Јури Кочетков/ЕПА)
Имунолошки (имунски) систем код човека
Људски организам је стално изложен бројним штетним агенсима у животној средини, међу којима важно место заузимају микроорганизми (бактерије, вируси, паразити, гљивице). Имунолошки (имунски) систем је одбрамбени систем организма који га штити од напада биолошких и хемијских агенаса, као и сопствених измењених (преканцерозних) ћелија, односно од свих чинилаца који би могли да наруше здравље. Имунитет је способност организма да се брани од њему страних или штетних материја које могу узроковати обољење, а када до болести дође утиче на дужину трајања болести и убрзава оздрављење. Имунитет је резултат садејства урођених фактора и фактора који се стичу током живота, на основу чега се разликују две компоненте овог система које се називају урођени (неспецифични) имунитет и стечени (специфични) имунитет. Захваљујући њиховом узајамном деловању људски организам поседује имунолошку толеранцију према ћелијама сопственог организма и развија имунолошку меморију према штетним агенсима који су већ били у контакту са организмом.
Урођени имунитет
Он представља прву линију одбране организма и то је отпорност коју организам поседује самим рођењем, дакле и пре контакта са узрочницима болести. Будући да подразумева исту реакцију према сваком штетном агенсу назива се и неспецифични имунитет. Под урођеним имунитетом подразумева се нпр. присуство трепљастог епитела (ћелије са ресицама) на слузници дисајних путева који задржава штетне честице и потискује их ван организма.
Стечени имунитет
Он се развија у контакту са различитим узрочницима болести, односно не постоји пре првог контакта са патогеним агенсом. У току инфекције специфични механизми одбране се јављају касније, када су микроорганизми савладали неспецифичну одбрану и продрли у унутрашњост организма. У зависности од начина како се стиче, стечени имунитет може бити активан и пасиван при чему активни и пасивни имунитет могу настати природним и вештачким путем. Постоје:
– пасивни природни имунитет – отпорност новорођене деце у зависности од антитела која су присутна у организму мајке (током интраутериног живота антитела из организма мајке прелазе у организам плода, а у постнаталном периоду путем млека);
– активни природни имунитет – отпорност после прележане болести или неприметних инфекција;
– пасивни вештачки имунитет – отпорност која се стиче после уноса готових произведених антитела како би се спречила инфекција или тровање;
– активни вештачки имунитет – отпорност која настаје током вештачког контакта са микроорганизмима имунизацијом (вакцинацијом).
Имунски апарат
Имунски апарат се састоји од лимфног ткива распоређеног по целом телу, које се налази у тзв. лимфоидним органима као што су: коштана срж, тимус, лимфни чворови, крајници, слезина, кожа и слузнице. Сви они су међусобно повезани системом лимфних судова којим протиче лимфа. У њој се налазе лимфоцити, врста леукоцита (белих крвних зрнаца) који имају главну улогу у имунском одговору организма. Захваљујући мрежи лимфног система која се протеже целим организмом и која је повезана са циркулаторним системом, могућа је врло брза имунолошка реакција на било ком месту у телу. Дакле, за разлику од већине других органских система, имунолошки систем није локализован већ представља мрежу ћелија, ткива и органа који заједно делују у одбрани организма.
Коштана срж је најважније и највеће хематопоетско ткиво одрасле јединке. Највише је има у дугим костима, пршљеновима кичменог стуба и грудној кости. Главни је извор свих крвних ћелија, укључујући леукоците који постају ћелије имунолошког система.
Тимус је смештен у горњем делу грудног коша (иза грудне кости) због чега се назива и грудна жлезда. Представља главно место лимфопоезе где настају зрели лимфоцити тзв. Т- лимфоцити. Тимус је орган који први постаје лимфоидан у току развоја, наставља са растом после рођења достижући највећу тежину у пубертету, а потом полако атрофира и бива замењен масним ткивом. Из овог разлога највећа производња и диференцијација Т-лимфоцита је у детињству.
Лимфни чворови су жлезде смештене дуж сабирних лимфних судова и представљају филтер за ткивну течност на њеном путу ка лимфи. Има их 500-600 у целом организму, највише у пределу врата, препона, пазуха, стомака, грудног коша. Овалног су облика и нормално су величине 1- 2 цм, али се приликом инфекције увећају услед нагомилавања антитела. У циљу спречавања даљег ширења инфекције имунолошки одговор је најјачи на месту уласка антигена, тако су нпр. у случају запаљења ждрела, крајника или код инфективне мононуклеозе увећани лимфни чворови на врату, а у случају урогениталних инфекција на препонама.
Крајници се налазе симетрично на бочним странама средњег (усног) дела ждрела, док је аденоид (трећи крајник) сачињени од лимфног ткива смештен у горњем (носном) делу ждрела. Ждрелни крајници, аденоиди и језични крајник који се налази на корену језика заједно чине тзв. лимфни прстен (Валдејеров прстен), задужен за одбрану горњих дисајних путева и дигестивног тракта. Њихов задатак је да задржавају микроорганизме и друге штетне честице на самом уласку у организам, као и покретање имуног одговора у смислу лучења антитела. Ова функција је најважнија у првим годинама живота и има значајну улогу у матурацији (сазревању) свих лимфоидних органа.
Слезина је лоцирана високо у абдомену са леве стране, одмах испод дијафрагме. Има улогу сличну као и лимфни чворови, али се у њој одвија и разградња еритроцита (црвених крвних зрнаца) на крају њиховог животног века. За разлику од осталих лимфоидних органа, слезина нема лимфоток тако да ћелије и друге материје улазе у њу путем крви. Према томе, слезина представља филтер за крв и као таква реагује на све антигене присутне у крви.
Кожа је прва баријера за микроорганизме на путу из спољашње средине. Сама грађа коже је таква да не дозвољава продирање микроорганизама у организам домаћина. Масне киселине присутне у кожи утичу на њену pH вредност и бактерицидна својства. Поред тога, непатогене бактерије нормално присутне на кожи и стална измена површинског слоја коже спречавају колонизацију патогених микроорганизама.
Слузнице су, такође, прва линија одбране у спречавању продирања микроорганизама, посебно њихова грађа са трепљастим епителом горњих и доњих дисајних путева. Спречавању инвазије инфективних агенаса доприноси и секрет слузница који поред антибактеријских материја садржи и јоне неких метала нпр. цинка. Лимфно ткиво се налази у слузници респираторног, дигестивног и урогениталног тракта (MALT и GALT).
Лимфно ткиво слузнице (mucosa-associated lymphoid tissue –MALT) је дифузни систем малих концентрација лимфног ткива лоцираних у разним субмукозним (подслузничним) мембранама тела, као што је назофаринкс (горњи део ждрела), тироидни предео, груди, плућа, пљувачне жлезде, гастроинтестинални тракт и кожа. МALT је сачињен од Т и B- лимфоцита, али и плазма ћелија и макрофага које пресрећу антигене приликом проласка кроз епител слузнице. МАLТ изграђује око 50% лимфног ткива у организму и игра улогу у регулисању мукозног (слузничног) имунитета.
Лимфно ткиво црева (gut-associated lymphoid tissue-GALT) представља компоненту лимфног ткива слузнице (mucosa-associated lymphoid tissue-MALT) који има имунолошку улогу у спречавању ширења антигена у цревима. Захваљујући њеној физиолошкој функцији у апсорпцији хране, мукозна површина је танка и игра улогу пермеабилне (пропустљиве) баријере ка унутрашњости тела. Уједно њена осетљивост и пропустљивост чине је подложном инфекцијама, па тако, заправо, велика већина инфективних агенаса напада људско тело користећи овај пут. Функционални значај лимфног ткива црева у одбрани тела почива на великом броју плазма ћелија које оно поседује, а које су произвођачи антитела и чији број премашује број плазма ћелија у слезини, лимфним чворовима и коштаној сржи заједно.
Ту се такође налази и лимфоток који пролази кроз ткиво и повезује се са мезентеричним лимфним чворовима (дуж крвних судова стомака), тако да су и GALТ и мезентерични лимфни чворови станице где започиње имунски одговор захваљујући присуству имунолошких ћелија слузнице и подслузнице црева. GALТ такође обухвата и Пајерове плоче танког црева. Нова истраживања показују да GALТ може бити главно место за активност ХИВ-а, иако би одговарајући третман редуковао број ХИВ-а у периферној крви.
Лимфоцити се примарно стварају у коштаној сржи од ћелија претходница, након чега једна популација ћелија сазрева у тимусу (Т- лимфоцити), док друга сазревање завршава у коштаној сржи (B- лимфоцити) и активира се у лимфним чворовима. Зрели Т и B- лимфоцити потом прелазе у крв, а из крви у периферне лимфоидне органе где су увек присутни и спремни да реагују на штетне агенсе. Т- лимфоцити имају улогу да препознају и разликују стране материје од оних које припадају организму и да их униште, док B- лимфоцити регулишу стварање антитела. Након реакције са антигеном неке ћелије умиру, међутим, доста B-лимфоцита преживи и памти антигене односно структуру честица које су биле у контакту са организмом и ти B-лимфоцити могу стварати антитела која су специфична за тај антиген, ако се антиген поново појави у организму.
Антигени (имуногени) су супстанце које у организму изазивају имунски одговор и реагују са продуктима тог одговора преко одређених хемијских структура присутних на површини молекула. Ове структуре одређују специфичност антигена тј. одређују са којим антителом ће реаговати антиген. Да би нека супстанца била имуногена она мора бити веће молекулске масе и сложене хемијске грађе, али пре свега мора бити страна организму.
Антитела су врло хетерогена фамилија високоспецифичних протеина који се називају имуноглобулини. Настају у хуморалном имунском одговору, синтетишу их плазма ћелије које се стварају након стимулације B- лимфоцита антигеном. Налазе се у крви, секретима и другим телесним течностима.
Реакцијама између антигена и антитела организам се брани од инфективних агенаса и сопствених измењених, малигних ћелија. Међутим, реакције антиген-антитело су одговорне и за настајање бројних обољења (алергија, аутоимуне болести).
Извор: Народна мрежа
Шта је имунски одговор?
Имунски одговор је основна функција имунолошког система, која подразумева одговор Т и B- лимфоцита на антиген. Да би дошло до имунског одговора потребно је да антиген буде прерађен у организму, затим представљен имунокомпетентним ћелијама у најпогоднијем облику у коме га Т и B- лимфоцити могу препознати. Разликују се два типа имунског одговора: хуморални и ћелијски.
– Хуморални имунски одговор је одговор B- лимфоцита после реакције са антигеном и заснива се на стварању специфичних антитела, која се налазе у телесним течностима (хуморима) организма.
Након продора антигена у организам и његовог препознавања, B- лимфоцити се претварају у плазма ћелије које луче антитела против једног или више антигена који су проузроковали имунолошку реакцију. Поред плазма ћелија, током хуморалног одговора настаје и друга популација ћелија које се називају меморијске ћелије или памтилице (B2- лимфоцити), а које, за разлику од плазма ћелија, имају дуг живот. Приликом поновног продора истог антигена у организам меморијске ћелије се активирају, брзо се размножавају и претварају у плазма ћелије које луче велике количине специфичних антитела. Ћелије меморије и антитела имају способност да зауставе размножавање узрочника болести чим уђе у организам, односно пре развоја симптома болести. Хуморални имунски одговор је посебно значајан код бактеријских инфекција.
– Ћелијски (целуларни) имунски одговор је одговор Т- лимфоцита на антиген, при чему настају два типа ћелија: сензибилисани Т- лимфоцити који синтетишу и излучују цитокине (лимфокине) одговорне за запаљење (инфламацију) и цитотоксични Т- лимфоцити или лимфоцити убице који убијају циљане ћелије. Оба типа ћелија оштећују ткиво, цитотоксични Т- лимфоцити директно, док сензибилисани Т- лимфоцити то чине посредством запаљенске реакције. Ћелијски имунски одговор је значајан код вирусних и гљивичних инфекција, малигних тумора, трансплантације органа.
Антитела
Постоји пет класа антитела (имуноглобулина Ig): IgG, IgА, IgМ, IgЕ и IgD, које се разликују по величини молекула, хемијском саставу, антигенској специфичности, физичким и биолошким својствима.
Имуноглобулин G (IgG) је главни имуноглобулин, који чини 70-75% свих имуноглобулина у крви човека. Синтетише се у великим количинама током секундарног имунског одговора. Због релативно малих молекула, IgG пролази кроз плаценту у фетус и обезбеђује главну линију одбране од инфекција у првим недељама живота. Такође, IgG дифундује (пролази) из крвних судова у екстраваскуларне просторе и има способност да неутралише бактеријске токсине и вирусе.
Имуноглобулин А (IgA) чини 10-20% свих имуноглобулина у крви човека. IgA се налази у крви и свим секретима: пљувачки, сузама, носном секрету, мајчином млеку, секрету бронхија и цревног тракта, а посебан значај има за локални имунитет слузница респираторног и дигестивног тракта. Новорођенчад добијају секреторни IgА путем мајчиног млека чиме стичу пасиван имунитет у односу на гастроинтестиналне инфекције. Селективни дефицит IgА је релативно чест и повезује се са учесталим респираторним инфекцијама, али и алергијама и аутоимуним болестима.
Имуноглобулин М (IgМ) чини 10% свих имуноглобулина у крви човека. Многа природна антитела припадају IgМ класи имуноглобулина. У току имунског одговора IgМ се први синтетише од свих имуноглобулина. Због великих молекула IgМ не пролази кроз плаценту и слабо дифундује кроз зидове крвних судова, тако да своју активност испољава углавном интраваскуларно. Поред тога, IgМ се налази у секретима слузница заједно са IgА где има улогу у локалној одбрани од инфективних агенаса.
Имуноглобулин Е (IgЕ) се налази у незнатним количинама у крви човека, али се налази на мембрани базофилних гранулоцита и мастоцита. Ова класа имуноглобулина чини основ нормалног хуморалног имунског одговора на инфекције паразитима, али је и основ реакције преосетљивости типа 2, односно различитих алергијских болести. Због значаја који IgЕ има код алергијских реакција непосредно по остваривању контакта са антигеном који иницира алергију (значи са алергеном), повишене концентрације IgЕ у крви се јављају током алергијских обољења. Међутим, нормалне вредности IgЕ не значе да се алергијско обољење може и искључити, односно неопходна је интерпретација у комбинацији са осталим клиничким налазима.
Имуноглобулин D (IgD) се као и IgE налази у незнатним количинама у крви човека. IgD се заједно са IgМ молекулима налази на ћелијској мембрани лимфоцита где представљају рецепторе за антигене. Захваљујући њима долази до препознавања антигена и претварања B- лимфоцита у плазма ћелије које луче специфична антитела.
Квантитативно (количинско) одређивање имуноглобулина даје важне информације о хуморалном имунском одговору. У првом контакту са антигенима као примарна реакција у организму се појављују IgM антитела, а затим следи синтеза IgG и IgA. Повишене концентрације имуноглобулина у крви настају код акутних и хроничних инфекција, хроничних болести јетре, аутоимуних болести, плазмоцитома (мултиплог мијелома). Снижене концентрације имуноглобулина у крви се јављају услед смањене синтезе у урођеним и стеченим имунодефицијентним болестима или као последица губитка протеина код гастроентеропатија, опекотина, нефротског синдрома и слично.
Не треба се играти сложеним системом
Из свега овога се може извући закључак да је имунски систем човека веома сложен, да постоје бројни међузависни механизми који нас штите од свакодневних изазова и да ремећење или недостатак било које компоненте система води неповратно у болест. Ниједна функција ткива, органа, система органа или организма у целини не би била могућа без складног деловања имунског система.
Пандемија корона вируса нас је подстакла да више него икад размишљамо о свом имунитету, да га подстичемо и штитимо, али, такође, нас подсећа и на рањивост људског организма без обзира на то ком народу припадамо, у којој земљи живимо или да ли смо богати или сиромашни. Наметнула нам је и питање да ли смемо да будемо неодговорни према овако деликатном систему заштите који нам је Богом дан? Под тим не мислим само на појединачну одговорност, него и општељудску, цивилизацијску, па и научну. Да ли смемо оправдавати покушаје свесног или несвесног ремећења имунског система скривеног у новим технологијама које се примењују у биомедицинским испитивањима, генетском инжењерингу или лечењу појединих обољења? Да ли су и нове вакцине, до скоро непознате широј стручној јавности, део ремећења природне хомеостазе људског организма?
Медицинска наука сваким даном све више и боље упознаје функционисање људског организма. Сведоци смо бројних открића која омогућавају ефикасније лечење одређених врста обољења, али и даље постоје бројне непознанице које нас лимитирају или, можда, опомињу.
Зато смо дужни да поставимо питање и о новим вакцинама.
Нова технологија генетског модификовања
CRISPR–Cas 9 је технологија која се однедавно користи у генетском модификовању за брзо, лако и јефтино сечење генома на тачно одређеним локацијама.
CRISPR је скраћеница од „clustered regularly interspaced short palindromic repeats“ или, у слободном преводу, „груписана кратка палиндромска понављања на једнаким растојањима“ и односи се на места у геному где се ДНК секвенца понавља. Поред ових секвенци налазе се гени који кодирају синтезу ензима. Cas 9 је ензим нуклеаза који сече нуклеинске (ДНК/РНК) киселине.
CRISPR–Cas 9 је заправо систем који користе бактерије у одбрани од вируса.
О чему је реч?
Када вирус нападне бактерију он убацује свој генетски материјал с циљем да искористи бактерију за сопствену репликацију. Као одговор на то бактерија производи Cas ензиме који секу убачену вирусну нуклеинску киселину и делове инкорпорише у свој геном, управо на CRISPR местима. Следећи пут када иста врста вируса нападне бактерију, CRISPR места се заједно са инкорпорираном вирусном нуклеинском киселином преписују у РНК молекуле. Резултат тога је комплекс Cas 9 ензима и РНК молекула, РНК молекул методом поклапања секвенци идентификују вирус, а Cas 9 ензим сече препознату вирусну нуклеинску киселину на тачно одређеном месту.
Откриће и примена
Године 2012. Jennifer Doudna (Беркли Универзитет) и Emmanuelle Charpentier (Умеа Универзитет) су уз мање модификације поставиле темељ за употребу овог система у генетском инжењерингу. Убацивањем Cas 9 ензима са тзв. РНК водичем у ћелију, може се исећи било који део генома. Ћелија ће потом покушати да изврши репарацију оштећеног. Обзиром да је процес репарације склон грешкама може бити вођен и споља, убацивањем Тројанског коња, тј. секвенци ДНК, исправних или тотално другачијих од првобитних. За убацивање Cas 9 ензима са РНК водичем у ћелију најчешће се користе вируси.
Метода се може користити у биомедицинским истраживањима, од проучавања функције гена, мутација, у развоју и унапређивању лекова, дијагностичких метода, развоју нове платформе вакцина, куративно, па све до жељеног уређивања генома ембриона …
Јако важно је нагласити да се ова метода може користити како у in vitro тако и у in vivo условима; и како на соматским тако и на герминативним ћелијама (промене на герминативним ћелијама – сперматозоидима и јајним ћелијама би самим тим постале и наследне!).
Фантастично! А у чему је проблем?
У чему је проблем?
Проблем је што у свету жедном сензационалистичких научних открића недостају усаглашене етичке норме и законске регулативе. На пример, у Канади и Европи званично није дозвољено експериментисање на хуманим ембрионима, САД то не забрањује, док Кина има либералније регулативе. (овде) Такође, незамисливо је да се метода примењује in vivo на људима без претходне добре провере ефикасности и дугорочне безбедности. Како и сама ауторка методе наглашава – ова метода сама по себи није тешка, али је тешко њоме извршити генетско модификовање добро и безбедно. Јер, генетика је врло крхка равнотежа! (овде)
Примена у Кини и на Интернету
Убрзо након открића технологије, и пре него што је научно доказано да је ефикасна и безбедна за примену код сисара, група кинеских истраживача примењује CRISPR-Cas 9 методу на неимплантираним хуманим ембрионима, носиоцима гена за бета таласемију, добијених in vitro фертилизацијом. Техника се у овом случају испоставила прилично несигурном, обзиром да је ДНК секвенца релативно успешно измењена код мање од четвртине ембриона. (овде)
И док озбиљни научници упозоравају, Амазон већ доставља опрему за уређивање бактеријског генома на кућну адресу, веома повољно. (овде)
Генетска револуција
Појављују се заговорници који у овој методи виде нову, генетску револуцију, од могућности „безболесног“ и дуговечног живљења, до могућности креирања потомства по жељи. Ново доба – камено, бронзано, гвоздено, па све до генетског доба. У једној научној сесији посвећеној CRISPR-Cas 9, Jamie Matzl (биографија импозантна – од биотехнолошког експерта, геополитичара, оснивач One Shared World организације, писца футуристичких романа – „Хаковани Дарвин“, члана Клинтон–Бајден тима… (овде, овде, овде, овде)) изјављује, цитирамo: „у будућности, све више и више породица ће потомство добијати методом IVF (in vitro фертилизацијом – вештачком оплодњом), све више и више ће се радити генетски скрининг пре имплантације ембриона, и ми, као врста, ћемо бити ти који уређују гене својих ембриона, то ће бити за 10, 20 година, али свакако је незамисливо да ћемо за 100 година правити бебе на начин на који их сад правимо.“ На реторичко питање да ли ће то довести до нове поларизације код богатих и сиромашних, неуробиолог и биоетичар професор William Hurlbut констатује: на жалост то ће бити деца сиромашнијих, јер то су родитељи који желе да експериментишу.
Светска здравствена организација и јуриш на наше гене
Изјаве Jamie Matzlа можда и не би биле толико забрињавајуће да дотични није и у Управном одбору за развој глобалних стандарда за управљање и надзор људског генома при Светској здравственој организацији (СЗО). Тај исти одбор ових дана (објављен позив за допринос до 19. августа 2020.) доноси препоруке на основу којих ће СЗО прописати регулативе за управљање хуманим генетским модификовањем, и на глобалном и на локалном нивоу. (овде)
У самом уводу последњег доступног предлошка (од 3.7.2020) назначено је да је током рада овог одбора свет суочен са SARS-CoV2 пандемијом, а како се показало да генетско модификовање има важну улогу у решавању ове кризе, од разумевања болести, преко развоја дијагностичких метода, па све до развоја вакцина, постоји ургентна потреба за уређењем овог простора. (овде)
Идеолог генетске револуције
Да бисмо ближе приказали како западни свет гледа на ову проблематику преносимо још нека размишљања Jamie Matzlа (ако нисте гледали серију „Кула од карата“ можда ће вам бити тешко да схватите улогу и значај лобиста, што дотични свакако јесте, обзиром да не постоји научна сесија и конгрес на дату тему без његовог присуства):
„SARS епидемија 2003. год., птичији грип 2009. год., MERS 2012. год. и SARS-CoV2 2019. год., ово би требало да нам пружа довољно доказа да је још опаснија глобална пандемија на помолу… Научници већ истражују могућност генетског модификовања, било постојеће људске популације, било преимплантираних ембриона, да би повећали отпорност како од овог, тако и од других вируса… Ако вирус расте и мутира у сиромашним земљама у којима је лош здравствени систем, и људи у богатијим земљама ће касније трпети последице; наше здравље и благостање зависи и од других у нашем екосистему, па помажући другима заправо улажемо у себе…“ (овде, овде)
Дотични јасно каже: потребна нам је генетска модификација да бисмо избегли будуће пандемије.
Какве то везе има са обавезном вакцинацијом
Осврнимо се на садашњу пандемију и горућу тему – обавезну вакцину. За дугорочно гледано безбедну вакцину потребне су године истраживања и тестирања пре примене, али и повратне информације након много година употребе. Изазов је направити баланс ефектна / безбедна вакцина. Постоји толико инфективних агенаса и толико, до у најмањи детаљ познатих последичних инфективних обољења за која деценијама не успевамо да направимо адекватну вакцину. Сада имамо пандемију, вирус који брзо мутира /не мутира, оставља имунитет/не оставља имунитет, од асимптоматских до ширег дијапазона симптома, први талас/ први пик у првом таласу – и неколико вакцина у завршним фазама тестирања, после само седам месеци од идентификовања секвенци вируса. Према званичним подацима СЗО тренутно је преко 160 кандидата у трци за потенцијалну вакцину, и било би пожељно да вакцина после једне, евентуално две дозе, постигне заштиту која ће трајати најмање 6 месеци. (овде)
Трећа фаза испитивања
У тренутку писања овог текста неколико вакцина улази у трећу фазу истраживања којом треба да се на већој популацији испита да ли је имунолошки одговор који је изазван вакцином суфицијентан да заштити од појаве COVID–19. Осврнућемо се на вакцине које предњаче – оксфордска ChAdOx1-nCoV19, руска Gam-COVID-Vac и кинеска Ad5-nCoV. (овде, овде, овде) Све наведене, припадају новој, алтернативној платформи конвенционалним вакцинама, тзв. векторским вакцинама за које се тврди да су потентније, да се брже развијају, али и да им је производња финансијски приступачнија. Па да кренемо редом.
Векторске вакцине
Шта су то векторске вакцине? У векторски вирус уграђује се ген који кодира синтезу и експресију жељеног антигена на вектором таргетираној ћелији вакцинисане особе (слика у прилогу). Као вектор често се користи аденовирус због неких погодности његовог профила – политропизма (може да инфицира више ткива – око, респираторни, гастроинтестинални епител…), доброг индуковања и хуморалног и целуларног имунитета (не захтева додавање адјуванса), и безбедности (не изазива озбиљнију клиничку слику код имунокомпетентних). На основу способности векторског вируса да се репликује у циљаној ћелији, ове вакцине могу бити репликујуће или нерепликујуће, при чему репликујуће изазивају бољу имуну реакцију, али су мање безбедне, док су нерепликујуће теоретски безбедније, али је имуни одговор слабији. У случају горе наведених корона вирус вакцина, у векторски аденовирус убачен је ген корона вируса који кодира синтезу антигена тј. spike-протеина из његовог омотача (овај протеин се везује за ACE 2 рецептор хуманих ћелија и омогућава вирусу да инфицира ћелију). Векторски вирус уноси наведени ген у таргетиране ћелије вакцинисане особе које потом производе и презентују овај антиген имуном систему изазивајући имуну реакцију.
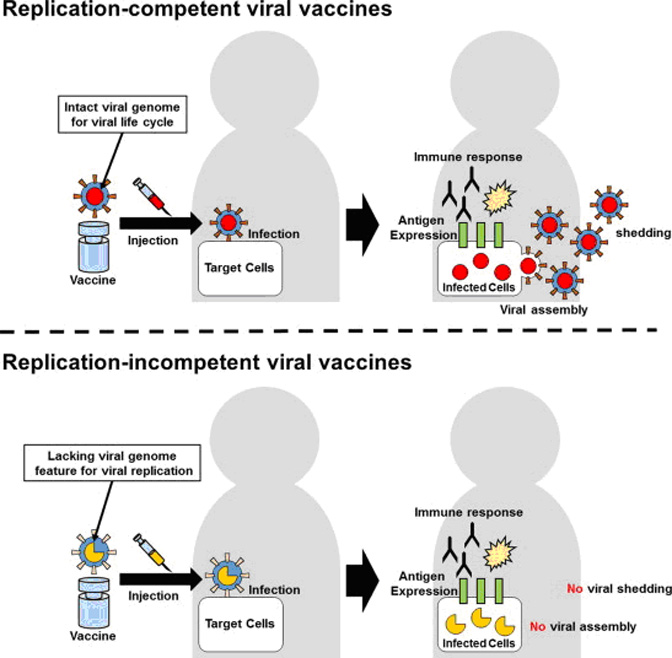
Репликујуће и нерепликујуће векторске вакцине
Само две одобрене вакцине до сада
Иако се, више од деценије, у многим светским лабораторијама интензивно ради на овој и сличним типовима вакцина, до 2019. године одобрене су само две за хуману употребу – Dengvaxia (против денге) и Imojev (против јапанског енцефалитиса). (овде)
Детаљнија анализа резултата истраживања, који и те како знају да изненаде, говори да је наше клиничко искуство о безбедности и ефикасности ове врсте вакцина још увек ограничено. Резултати студије која је обухватала 35000 испитаника управо за одобрену Dengvaxia вакцину, показали су да је ефектна у превентирању симптома код 76% особа, узраста 9 до 16 година, а за које је лабораторијски доказано да су пре вакцинације већ били заражени једним од серотипова денге (постоје четири серотипа, када се особа зарази једним – од тог серотипа постаје доживотно заштићена, а на преостала три постоји краткорочни унакрсни имунитет, након тога инфекција неким од преостала три серотипа може довести до тешке клиничке слике и смртности).
Денга: опасније ако си вакцинисан
У Америци наведена вакцина није одобрена за оне који никад нису били инфицирани било којим серотипом поменутог вируса и који не живе у ендемским жариштима. Зашто? Јер се показало да вакцина опонаша примоинфекцију, па је инфекција вирусом након вакцинације имала два пута већи ризик за развој теже клиничке слике код вакцинисаних у поређењу са невакцинисанима. Клиничка студија је обухватала и децу и труднице. (овде, овде)
Друга, STEP и Phambili студија за аденовирус векторску HIV вакцину је необјашњиво као резултат имала виши степен HIV позитивних међу вакцинисаним него у невакцинисаној контролној групи, па је студија убрзо обустављена. (овде) Каснијом анализом дошло се до закључка да је код оних који су пре вакцине имали развијен имунитет на аденовирус који је коришћен као вектор – вакцинација довела до пораста меморијских CD 4+ Т ћелија у слузници, а управо њих HIV и напада. (овде)
„Цитокинска олуја“ представља непредвидиву, неконтролисану, јаку реакцију урођеног имунитета на неке инфективне (најчешће вирусне) и неинфективне агенсе, са појачаним ослобађањем одређених проинфламаторних медијатора – цитокина, чиме доводи до озбиљних мултисистемских оштећења. (овде) Немали број радова сведочи да је управо цитокинска олуја одговорна за значајан број смртних исхода код оболелих од корона вируса а који су били без коморбидитета. (овде) А, са друге стране, познато је да је и хумани аденовирус (који се користи као вирусни вектор) потенцијално потентни активатор цитокинске олује (праћене и дисеминованом интраваскуларном коагулацијом…), са такође значајним бројем објављених радова који указују на ову проблематику. (овде, овде)
Да ли постоји опасност код пацијената са хроничним вирусним инфекцијама?
По мишљењу неких од експерата СЗО, нека питања од критичног значаја, попут питања о рекомбиновању вирусног вектора са дивљим патогеним сојевима такође остају недоречена. (овде) Вирусни вектор може стећи вируленцију и in vivo, или се може рекомбиновати са ендогеним вирусима, или са дивљим сојевима, или уколико дође до контаминације током производње. Обзиром да сe пацијенти са хроничним вирусним инфекцијама (hep B, hep C, HIV itd.) најчешће искључују током испитивања ових вакцина, да ли су оне безбедне и за њих? Не заборавимо да СЗО даје податак да тренутно око 250 милиона људи у свету има хронични хепатитис Б (hep B) , а од тога око 27 милиона (10%) није ни свесно да је инфицирано. Па, да ли се испитује безбедност истовременог примања новог типа вакцина са другим вакцинама из редовног календара, нарочито са тзв. живим вирусним вакцинама (MMR)?
Код репликујућих векторских вакцина постоји и потенцијал за ширење вируса са вакцинисаних на невакцинисане, нарочито имунокомпромитоване. Ове вакцине могу бити патогене за имунокомпромитоване, а они су заправо и најугроженија популација током епидемија. Још један од проблема је помињано постојање имунитета на вирусни вектор пре вакцинације, чиме се доводи у питање ефикасност вакцине, а вакцинисани при том има лажну слику да је заштићен. (овде)
Постављамо питања
Како проблем развијеног имунитета на вирусни вектор може настати и код ревакцина или код употребе друге вакцине која користи исти вектор, прибегава се потенцијалној употреби анималних аденовируса као вектора. (овде) Ако хумани аденовирус Ad 12 има онкогени потенцијал код глодара, да ли смо сигурни да неки од анималних серотипова нису онкогени за људе? (овде)
Иако примена вирусних вектора има све већу и значајнију улогу и у терапији аутоимуних и онколошких обољења, намеће се и контра питање – да ли трансгени касније могу имати улогу у етиогенези неких аутоимуних болести код вакцинисаних? (овде)
Констелацијом наведених примера и низа питања желимо да прикажемо о колико комплексном механизму се ради. Иако је напредак у овој сфери науке неспоран, неспорно је и непотпуно разумевање свих компонената у функционисању људског имунолошког система. Отуд и објективни разлози за забринутост. На многа питања треба дати одговоре пре него што се еуфорично стане у ред за грабљење вакцине и укључивање трећине своје популације у експеримент.
Примаријус др Милан Рогановић, др Марта Ковачевић
НАПОМЕНА: Ранија верзија овог текста грешком није садржавала пасус који почиње са „Цитокинска олуја…“, у поглављу „Денга: опасније ако си вакцинисан“ (29. 8. 2020)
Categories: Аз и буки

Оставите коментар